L’objectif de cette série de mémos est d’apporter les données scientifiques montrant que réduire l’exposition aux Perturbateurs Endocriniens permet de réduire l’impact des grandes maladies chroniques, parfois dans un délai assez rapproché. La 1ère est consacrée à une maladie infantile encore largement ignorée le MIH.
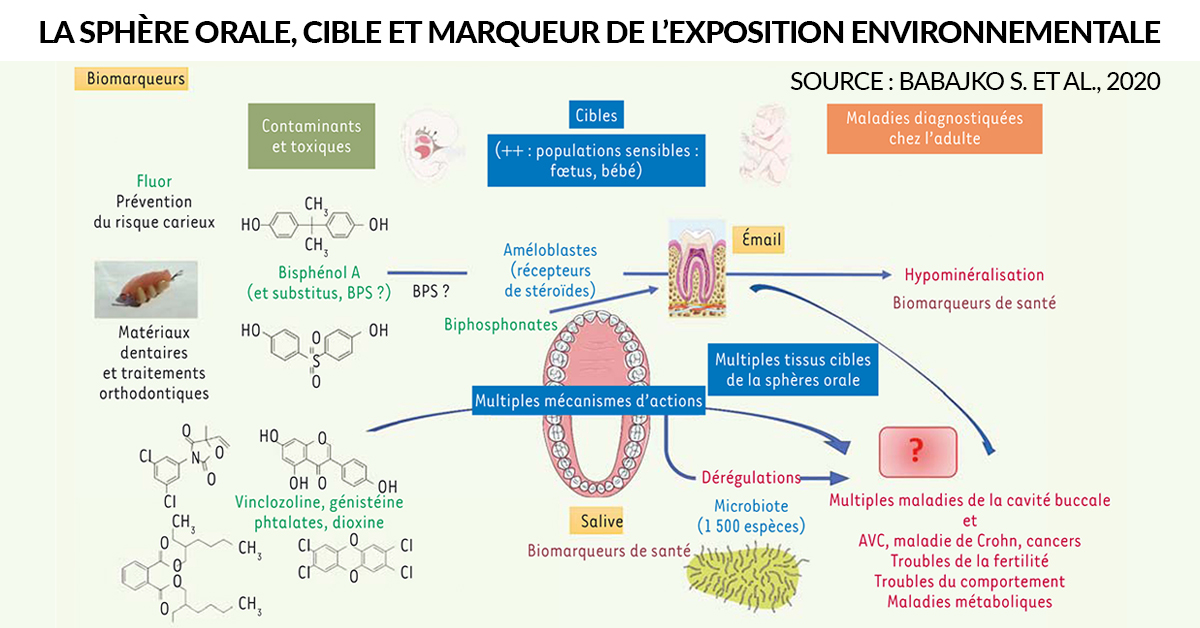
Dr Alice BARAS, chirurgien-dentiste spécialisée en promotion de la santé environnementale, rappelle que la sphère orale est cible et marqueur de l’exposition environnementale.
La transition épidémiologique figurée par l’épidémie mondiale de maladies chroniques (OMS 2006) s’explique en grande partie par une évolution défavorable de plusieurs facteurs environnementaux. Ces déterminants de santé entrainent notamment une mutation des risques sanitaires liés à la révolution chimique et la pollution des milieux qu’elle entraîne [1].
Les enjeux de santé publique en lien sont majeurs. La promotion de la santé environnementale est incontournable et est un défi quotidien à relever. Cependant, l’impérieuse nécessité de développer la sensibilisation et la formation des professionnels de santé à cette discipline grâce à son intégration transversale au sein de leur formation initiale et continue reste sans application concrète. Ceci malgré le fait qu’elle ait été objectivée dans plusieurs textes officiels tels que les Plans Santé Environnement, la 2ème Stratégie Nationale sur les Perturbateurs Endocriniens, la Stratégie Nationale de Santé, le 3ème Plan santé Travail ou encore la Déclaration d’Ostrava (OMS, 2017).
Parmi les professionnels de santé, les chirurgiens-dentistes sont concernés à plus d’un titre. D’une part, en étant acteur du dépistage précoce de maladies liées à l’environnement, d’autre part par la nature même de leur activité et l’exposition aux risques chimiques qu’elle peut entraîner.
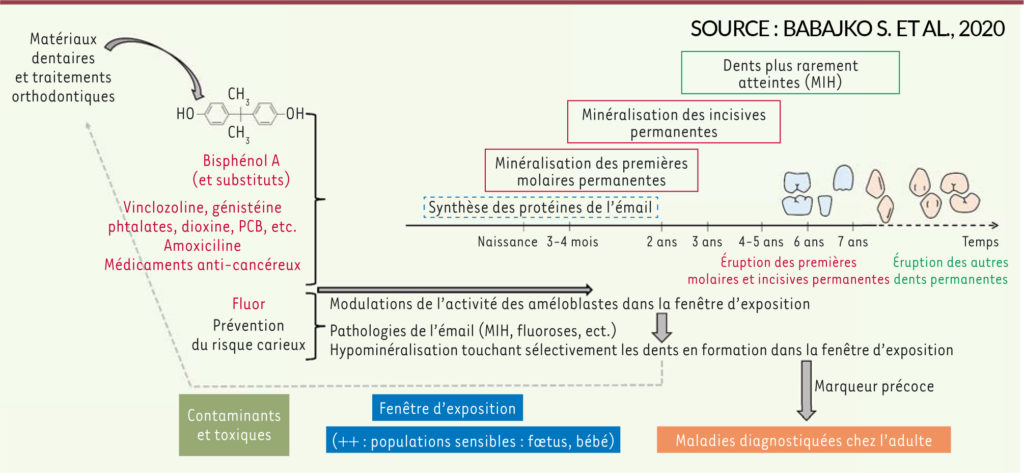
En effet, comme le souligne la synthèse publiée récemment par une équipe de chercheurs issus de différents Instituts et Universités de France, la sphère bucco-dentaire est la cible et le marqueur d’exposition à de nombreux facteurs environnementaux. L’observation et la compréhension précise des interactions de cet écosystème pourront alors aider à prévenir de nombreuses pathologies orales et générales (Babajko S. et al., 2020) [2].
Parmi ces pathologies, le chirurgien-dentiste est particulièrement confronté à l’émergence rapide de l’une d’entre elles : L’Hypominéralisation des Molaires et Incisives (MIH). Sa description clinique ne date que de 2001. Elle est caractérisée par la présence de tâches opaques irréversibles de l’émail des molaires et incisives définitives. L’établissement du diagnostic précoce est primordial, car une thérapeutique adaptée et efficace doit être mise en œuvre le plus rapidement possible afin d’éviter l’échec thérapeutique.
D’un point de vue épidémiologique, la dernière méta-analyse parue met en évidence une prévalence mondiale de MIH de 14,2% (Zhao D. et al. 2017) [3] pouvant varier selon les études et les pays dans lesquels elles sont menées de 2,9 à 44% (Elfrink ME. Et al. 2015) [4]. L’explication histologique est une altération de la fonction des améloblastes lors de la phase de maturation de l’émail entre le dernier trimestre de la grossesse et les premiers mois de la vie de l’enfant(Jalevik B. et al., 2005) [5] [6].
Concernant l’étiologie du MIH, les hypothèses avancées dans la littérature odontologique sont multiples et font état d’une origine multifactorielle systémique : une possible hypoxie à la naissance, de fortes fièvres, des infections ORL fréquentes ou encore une exposition périnatale aux perturbateurs endocriniens (Courson F. et al., 2017) [7]. Cette dernière hypothèse a été appuyée par une étude expérimentale menée sur des rats exposés quotidiennement à de faibles doses de Bisphenol A (BPA). Des tâches opaques et blanches sont apparues sur les dents des rongeurs. L’analyse de ces défauts montre qu’ils partagent de nombreuses caractéristiques structurales et biochimiques avec ceux décrits dans le MIH. Les résultats suggèrent que le BPA, et les perturbateurs endocriniens empruntant les mêmes voies d’action, pourraient faire partie des agents causaux de cette pathologie [8] (Jedeon et al., 2013) [9].
Ces études sont particulièrement intéressantes à exploiter en considérant alors le MIH comme un marqueur précoce d’exposition au BPA. Le dépistage précoce du MIH chez l’enfant favoriserait ainsi le déploiement d’une surveillance accrue des jeunes patients atteints et les moyens d’une prévention secondaire.
L’information des familles et des professionnels de santé permettrait de favoriser une vigilance sur les symptômes associés à une puberté précoce ou le dépistage de cancers hormono-dépendants ou répondre de manière adaptée à un trouble du comportement éventuellement observé chez ces enfants (Le Houezec et al., 2015) [10]. La recherche fondamentale et l’étude de larges cohortes apporteront probablement des éléments supplémentaires de compréhension.
De par leur activité, les chirurgiens-dentistes sont en contact permanent avec des produits chimiques. Certains sont classés Cancérigènes Mutagènes Reprotoxiques (CMR) [11], neurotoxiques, perturbateurs endocriniens, comme le fluor ou le mercure [12]. Certains matériaux de collage et reconstitution sont susceptibles de libérer des monomères de BPA (Dursun et al., 2016) [13]. L’utilisation à but thérapeutique ou préventif des nanomatériaux soulève également la question du manque de recul sur le risque sanitaire associé, réaffirmé par l’ANSES [14]. La constante évolution des techniques et des biomatériaux ne doit pas se faire au détriment de la santé du chirurgien-dentiste et de son équipe soignante, ni de celle des patients et de l’environnement.
[1] La production chimique, inexistante au début du 19e siècle, a été multiplié par 1000 depuis 1930. Elle représente aujourd’hui 1 milliard de tonnes par an et plus de 100 000 substances commercialisées différentes.
[2] Babajko et al., 2020. « La sphère orale, cible et marqueur de l’exposition environnementale ». Méd Sci (Paris) 2020 ; 36 : 225-230.
[3] Zhao D. et al. « The prevalence of molar incisor hypomineralisation : evidence from 70 studies ». Int J Paediatr Dent. Juil 2017.
[4] Elfrink ME et al. « Satndardised studies on Molar Incisor Hypomineralisation (MIH) and Hypomineralised Second Primary Molars (HSPM) : a need. Eur Arch Paediatr Dent 2015 ; 16 ; 247-55.
[5] Jalevik B et al. « Scanning electron micrograph analysis of hypomineralized enamel in permanent first molars ». Int J Paediatr Dent 2005, 15 (4) : 233-240.
[6] La minéralisation de l’émail commence au cours du troisième trimestre de vie fœtale et s’achève autour de la cinquième année après la naissance (sauf pour les dents de sagesse). Les cellules responsables de cette amélogènèse disparaissant au moment de l’éruption des dents, tout impact est irréparable et donc irréversible. Ces stigmates permettent de dater rétrospectivement la période d’exposition.
[7] Courson F. et al. « Hypominéralisation molaire-incisive ». EMC 2017, volume 12, n°5, octobre
[8] Suite à la publication de cette étude, un colloque au Sénat a été co-organisé par le Réseau Environnement Santé le 23/06/2016 autour du thème « vers une dentisterie sans perturbateurs endocriniens » afin de favoriser les échanges et la prise de conscience des enjeux en lien avec cette étude. https://www.reseau-environnement-sante.fr/wp-content/uploads/2016/06/Actes-du-colloque-Vers-une-dentisterie-sans-Perturbateurs-Endocriniens.pdf
[9] Jedeon et al. « Enamel defects reflect perinatal exposure to bisphenol A ». Am J. Pathol. 2013, 183 : 108-118.
[10] Le Houezec D. et al. « Le bisphenol A est « sur les dents » », Méd. Enf 2015, 347-351.
[11] Pépin E. et al. « Analyse des pratiques professionnelles dans les cabinets dentaires de Drôme Provençale : exposition aux rayonnements ionisants, aux agents biologiques et aux produits chimiques. » INRS 2014, santé au travail.
[12] Selon la TedX list https://endocrinedisruption.org/interactive-tools/tedx-list-of-potential-endocrine-disruptors/search-the-tedx-list
[13] Dursun et al., « Bisphenol A release : survey of the composition of dental composite resins. Open DentJ.2016 ;10 :446-453.
[14] ANSES, 2014 : « recommandations nanomatériaux ». https://www.anses.fr/fr/content/%C3%A9valuation-des-risques-li%C3%A9s-aux-nanomat%C3%A9riaux